Nieuwe studie zoekt naar erfelijke oorzaken van kinderkanker.
Auteur: Karolinska Institutet - medicalxpress.com/news
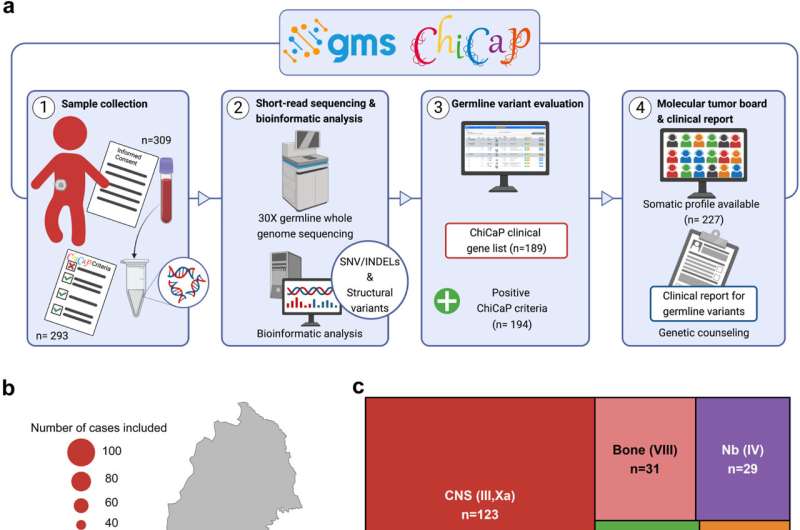
Overzicht van studieopzet en studiecohort.
Credit: The Lancet Regional H
"Onze resultaten zijn van grote klinische betekenis voor de manier waarop we de kinderen moeten opvolgen en ook hoe we ze moeten behandelen", zegt Ann Nordgren, hoofdonderzoeker, professor aan het Karolinska Institutet en senior arts bij Klinische Genetica en Genomica, Karolinska Universitair Ziekenhuis en de afdeling Laboratorium. Geneeskunde, Sahlgrenska Academie, Universiteit van Göteborg.
Veranderingen in de behandeling als gevolg van ChiCaP:
Een van de belangrijkste ontdekkingen is dat kiemlijnvarianten die verband houden met kinderkanker niet alleen helpen bij het inschatten van het risico dat andere familieleden kanker ontwikkelen, maar ook een op maat gemaakte follow-up en behandeling van de patiënt zelf mogelijk maken.
Patiënten met het Constitutional Mismatch Repair Deficiency (CMMRD)-syndroom, een genetische aandoening met een hoog risico op kanker bij kinderen, hebben bijvoorbeeld geïndividualiseerde surveillanceprogramma's en immunotherapie ontvangen als onderdeel van hun tweedelijnsbehandeling.
Impact op familie en broers en zussen:
Het ChiCaP-onderzoek heeft niet alleen een directe impact op de behandeling van de patiënt, maar heeft ook een aanzienlijke impact op het gezin. Het legt uit waarom hun kind kanker heeft en hoe eventuele risico's voor broers en zussen en andere familieleden in de toekomst kunnen worden beheerst.
Bianca Tesi, eerste auteur van de studie en gespecialiseerd arts bij Clinical Genetics and Genomics, Karolinska University Hospital, zegt: “Door vast te stellen of het kind een erfelijke oorzaak van kanker heeft, kunnen we ook weten of andere familieleden genetische counseling moeten krijgen en testen in de reguliere zorg.
"Dit kan belangrijk zijn omdat aan familieleden met een bevestigd risico soms specifieke screeningprogramma's kunnen worden aangeboden. Op dezelfde manier is het belangrijk geweest om bekende erfelijke factoren uit te sluiten om de zorgen over kanker onder familieleden te verminderen."
Een voorbeeld dat in de publicatie wordt beschreven, zijn broers en zussen van kinderen met retinoblastoom. Door een aanpak die resultaten uit genetische analyse van zowel bloed- als tumor-DNA gebruikt om het risico op broers en zussen te beoordelen, was het mogelijk om te identificeren welke broers en zussen gevolgd moesten worden in controleprogramma's en welke geen verhoogd risico op retinoblastoom hadden.
Als gevolg hiervan hoefden de broers en zussen zonder verhoogd risico gedurende de eerste vier jaar van hun leven geen uitgebreide controleprogramma’s met dertien oogonderzoeken onder algemene anesthesie te ondergaan.
"Dit is een nieuwe manier van denken in de oncogenetica die de risicobeoordeling van kanker voor andere kankerdiagnoses ten goede kan komen", zegt Bianca.
Gustaf Ljungman, een van de leidende onderzoekers, hoogleraar kindergeneeskunde aan de Universiteit van Uppsala, senior consultant in kinderoncologie aan het Universitair Ziekenhuis van Uppsala, en covoorzitter van de klinische groep op het gebied van GMS Kinderkanker, zegt: “Deze samenwerking tussen verschillende beroepen is cruciaal om te begrijpen en kinderkanker effectief behandelen.
"De ChiCaP-studie is van onschatbare waarde gebleken voor de ontwikkeling van de toekomstige zorg voor kinderkanker en zal inzichten en biologische kennis blijven opleveren die ons vermogen om kinderkanker te bestrijden zal verbeteren."
